2011年9月23日〜27日にスウェーデン・ストックホルムにて開催されたThe European Multidisciplinary Cancer Congress 2011 - ESMOより、大腸癌や胃癌などの注目演題のレポートをお届けします。演題レポートの冒頭には、臨床研究の第一線で活躍する監修ドクターのコメントを掲載しています。

切除不能進行・再発大腸癌既治療例に対するFOLFIRI + Aflibercept療法の検討:プラセボ対照無作為化比較第III相VELOUR試験の結果から
Results From VELOUR, a Phase III Study of Aflibercept (A) Versus Placebo (pbo) in Combination with FOLFIRI for the Treatment of Patients (pt) with Previously Treated Metastatic Colorectal Cancer (MCRC)
Josep Tabernero, et al.

切除不能進行・再発大腸癌2nd-line治療における新たな選択肢となる血管新生阻害薬Aflibercept

切除不能進行・再発大腸癌2nd-lineとして、FOLFIRI + AfliberceptがFOLFIRI + placeboに対して有意にoverall survival (OS) とprogression-free survival (PFS) を改善したという結果はすでに報告されていたが1)、本発表では層別因子、患者背景における、あらかじめ計画されていたサブグループ解析の結果が報告された。
1st-lineにおけるBevacizumab有無の解析ではOSにおいて未使用例でHR=0.788、既治療例でHR=0.862、PFSにおいてもそれぞれHR=0.797、HR=0.661であり、前治療のBevacizumabの有無にかかわらずAfliberceptの有効性が示唆されている。L-OHP ± Bevacizumab治療歴を有する切除不能進行・再発大腸癌に対してFOLFIRI + Aflibercept療法は有用であると考えられる。
しかし、1st-lineでBevacizumab未使用の2nd-lineについてはE3200 試験においてFOLFOXへのBevacizumabの生存上乗せ効果がすでに示されている2)。Aflibercept群はplacebo群に比べて下痢、倦怠感、好中球数減少が明らかに多いと報告されており、比較的毒性のmildなBevacizumabとどのように使い分けていくのかが課題となると思われる。 1st-lineでBevacizumabが無効となった場合の2nd-lineにおいても、KRAS 野生型症例ではPanitumumab、Cetuximabの有効性も示されている。今後、Bevacizumab beyond progression (BBP) の有効性を検証するAIO 0504試験3) やBBPと抗EGFR抗体薬を比較する試験の結果が出た後、2nd-lineでAfliberceptも含めた分子標的治療薬をどのように使い分けるかを再考していく必要があると思われる。
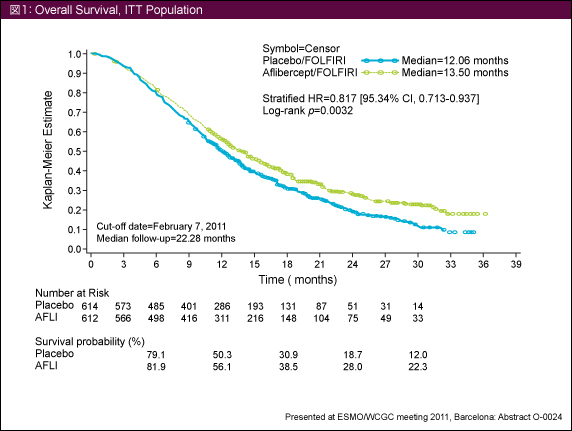
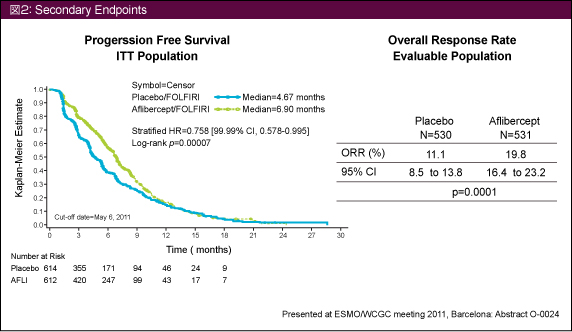
Afliberceptは、VEGF-AとVEGF-B、placental growth factor (PlGF) を阻害する新規の可溶性融合蛋白製剤である。本試験の主要結果は第13回世界消化器癌学会 (ESMO/WCGC 2011) において報告され、主要評価項目であるOSはAflibercept群で13.5 ヵ月、placebo群では12.06ヵ月と、有意な差をもってAfliberceptの有効性が証明された (HR=0.817, 95% CI: 0.713-0.937, p=0.0032)1) (図1)。PFSおよびORRにおいても同様であった (図2)。
今回はAfliberceptの頑健性 (Robustness) を検証するため、あらかじめ計画されていたサブグループ解析の結果を報告する。
今回はAfliberceptの頑健性 (Robustness) を検証するため、あらかじめ計画されていたサブグループ解析の結果を報告する。
対象はOxaliplatin (L-OHP) ベースの化学療法を施行された切除不能進行・再発大腸癌患者とした (試験デザインは図3参照)。下記のサブグループにおけるAfliberceptの治療効果を評価した。
治療効果と各サブグループ間の交互作用は両側10%として検証した。治療効果のHRと (1-α) %信頼区間はCox比例ハザードモデルを用いて算出した。さらに、Bevacizumab既投与症例における安全性の解析も実施した。
| ・ | 層別因子: ECOG PS (0/1/2)、前治療におけるBevacizumab投与の有無 |
| ・ | 患者背景: 年齢、性別、地域、高血圧の既往歴、転移個数、肝転移、原発巣の部位 |
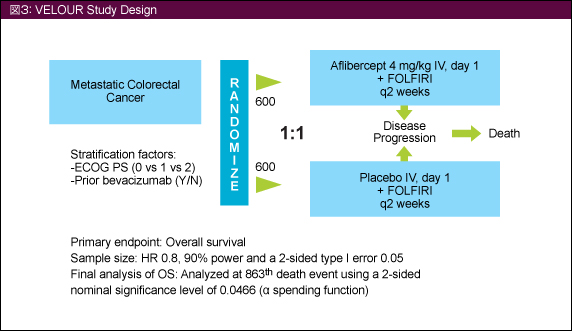
2007年11月‐2010年3月の間に1,226例が登録され、Aflibercept + FOLFIRI群(612例) とplacebo + FOLFIRI群 (614例) に無作為に割り付けられた。
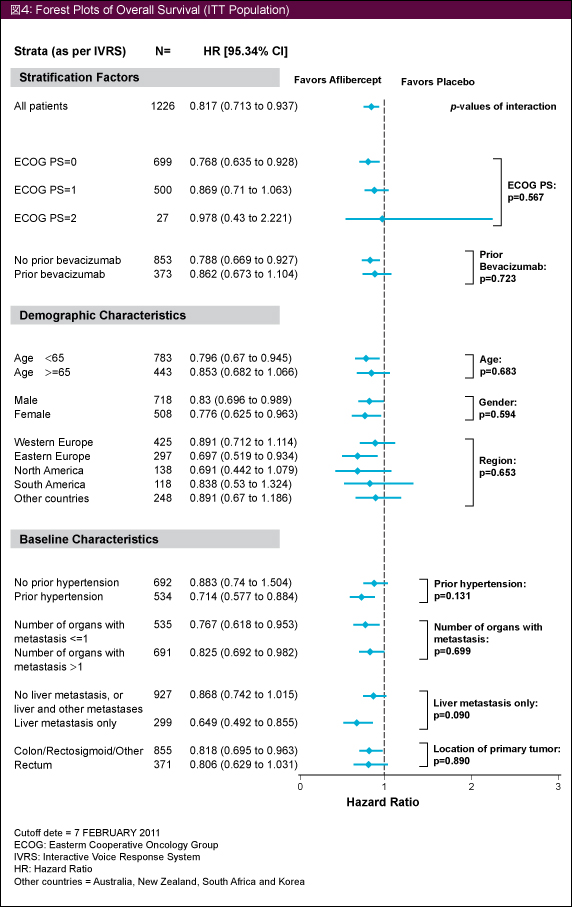
サブグループ解析の結果、ほぼ全てのドメインにおいて一貫したAfliberceptのOSにおける効果が認められた (図4)。肝転移の状態とAfliberceptのOSにおける効果との間には交互作用が認められ(p=0.090)、肝限局転移を有する症例ではそれ以外の症例 (肝外転移を有する症例、肝転移のない症例) よりも高い効果が得られた (それぞれHR=0.649 [95.34% CI:0.492-0.855]、HR=0.868 [95.34% CI: 0.742-1.015])。PFSにおいても同様であった。
サブグループ解析の結果、ほぼ全てのドメインにおいて一貫したAfliberceptのOSにおける効果が認められた (図4)。肝転移の状態とAfliberceptのOSにおける効果との間には交互作用が認められ(p=0.090)、肝限局転移を有する症例ではそれ以外の症例 (肝外転移を有する症例、肝転移のない症例) よりも高い効果が得られた (それぞれHR=0.649 [95.34% CI:0.492-0.855]、HR=0.868 [95.34% CI: 0.742-1.015])。PFSにおいても同様であった。
また、前治療におけるBevacizumab投与の有無による解析でも、OS、PFSともに交互作用はみられず、Bevacizumab既投与症例においてもAfliberceptが有効であることが示された (表1/図5)。
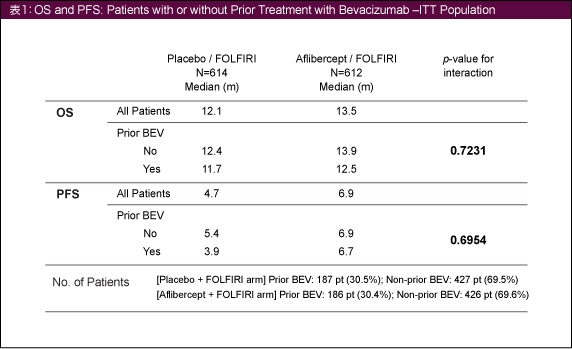
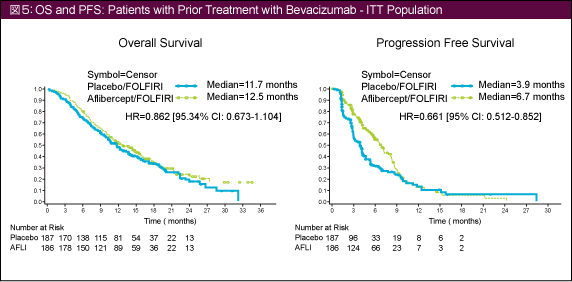
なお、Bevacizumab既投与症例と未投与症例におけるGrade 3/4の有害事象の発現頻度は、蛋白尿がそれぞれ8.6%、7.5%、高血圧16.6%、20.5%、静脈血栓塞栓症8.0%、7.8%、動脈血栓塞栓症2.1%、1.7%などであり、ほぼ同等であった。
Aflibercept + FOLFIRI療法は、L-OHPベースの化学療法を施行された切除不能進行・再発大腸癌患者に対し、OSならびにPFSを有意に延長した1)。さらに本解析結果より、Bevacizumab既投与症例を含むほぼ全てのドメインにおいて、一貫した効果を示したことが確認された。なお、前治療におけるBevacizumabの投与はAfliberceptの安全性プロファイルに有意な影響を与えないものと思われる。
Reference
1) Van Cutsem E, et al.: the 13th World Congress on GI Cancer (ESMO/WCGC 2011): Abst #O-0024
2) Giantonio BJ, et al.: J Clin Oncol. 25(12): 1539-44, 2007 [PubMed][論文紹介]
3) AIO 0504 (ClinicalTrials.gov): A Study of Avastin (Bevacizumab) Plus Crossover Fluoropyrimidine-Based Chemotherapy in Patients With Metastatic Colorectal Cancer.
1) Van Cutsem E, et al.: the 13th World Congress on GI Cancer (ESMO/WCGC 2011): Abst #O-0024
2) Giantonio BJ, et al.: J Clin Oncol. 25(12): 1539-44, 2007 [PubMed][論文紹介]
3) AIO 0504 (ClinicalTrials.gov): A Study of Avastin (Bevacizumab) Plus Crossover Fluoropyrimidine-Based Chemotherapy in Patients With Metastatic Colorectal Cancer.
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。

