背景と目的
切除不能進行・再発大腸癌のxenograft modelにおいて、HER2増幅は抗EGFR抗体薬であるCetuximab耐性の原因と考えられ1)、またTrastuzumabとLapatinibの単剤療法には反応しないが、併用療法には反応性を示すことが報告されている1)。そのため、HER2をdualに阻害する戦略としてHER2陽性切除不能進行・再発大腸癌患者に対するサルベージラインとして、TrastuzumabとLapatinibの併用療法の有効性と安全性を評価する第II相試験を実施した。
対象と方法
対象は、KRAS exon 2野生型、HER2陽性 (ICH2+および3+)、フッ化ピリミジン系製剤、Irinotecan (CPT-11)、Oxaliplatin (L-OHP)、Cetuximab、Panitumumabに不応なECOG PS 0/1の大腸癌患者であった。スクリーニングされた849例のうち46例 (4.8%) がHER2陽性であり、そのうち24例が登録され、23例が評価可能であった (図1)。薬剤投与量はTrastuzumab 2mg/kg/weekおよびLapatinib 1,000mg/dayであった。主要評価項目は奏効率、副次的評価項目は無増悪生存期間 (TTP) と安全性であった。
図1
結果
奏効率は34.7%、病勢コントロール率は78%で、CRが1例 (4.3%) に認められた (図2)。
図2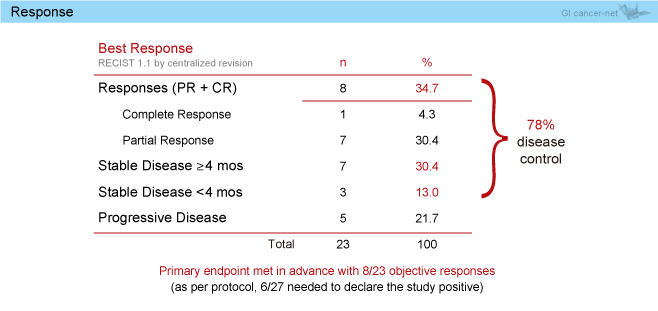
TTP中央値は、ITTでは5.5ヵ月 (95% CI: 3.7-9.8) であり、HER2 status別では3+で7.3ヵ月、2+で4.2ヵ月であった (図3)。
図3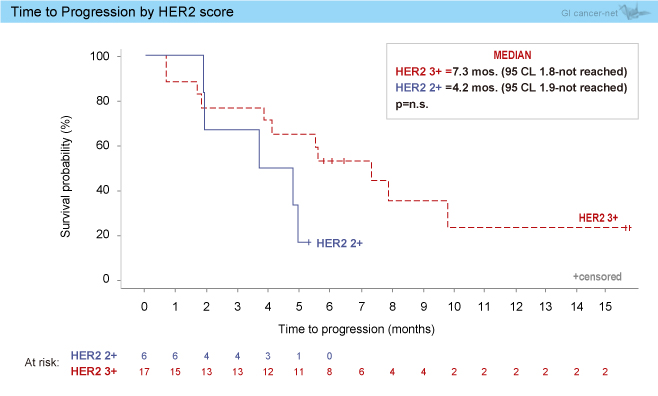
薬剤関連有害事象は、grade 3では倦怠感が3例、皮疹が1例に認められた (図4)。
図4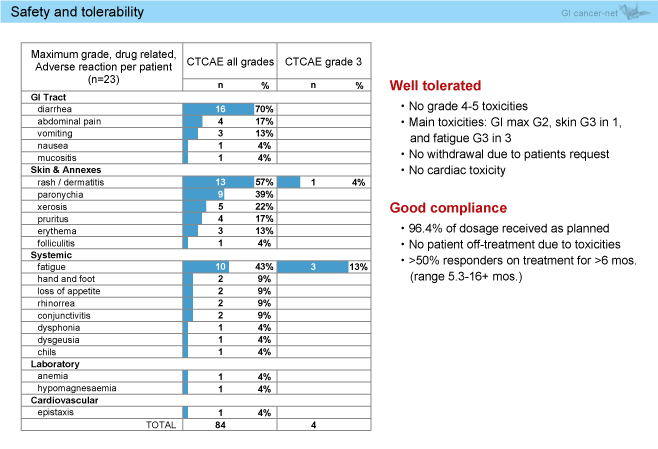
結論
本試験より、HER2陽性切除不能進行・再発大腸癌患者の奏効率は34.7%で、重篤な副作用が認められなかったことが示され、HER2のdual阻害は新しい治療オプションとして有望であると考えられた。
コメント
KRAS 野生型大腸癌のうちHER2陽性は5%を占めるのみで、しかも前治療不応の症例を対象としていることから、実際に試験に登録できた症例はその約半数であった。確かに効果は素晴らしいものであるが、xenograft modelをそのまま臨床に応用した研究であり、TrastuzumabもLapatinibも単剤での有効性は確認されていない。今後、HERACLES B試験としてPertuzumabとの併用も検討される予定がある。患者数そのものは非小細胞肺癌のALK 融合遺伝子陽性例と同等とのことであるので、ぜひ2剤併用の必要性も検討して、HER2陽性大腸癌に対する至適治療戦略を構築していただきたい。
(レポート:川崎 健太 監修・コメント:寺島 雅典)
- Reference
-
- 1) Bertotti A, et al.: Cancer Discov.?1(6): 508-523, 2011[PubMed]


