背景と目的
大腸癌はheterogeneityな癌であり、多くの研究グループがそれぞれ違う方法、異なった患者群で、遺伝子発現プロファイルによる大腸癌の分子サブタイピングを行っている (図1)。そこで、大腸癌分子サブタイプのコンセンサスの構築を目的に、参加する各研究グループに蓄積されたデータをまとめ、解析するためのコンソーシアムを作り、研究を行った。
図1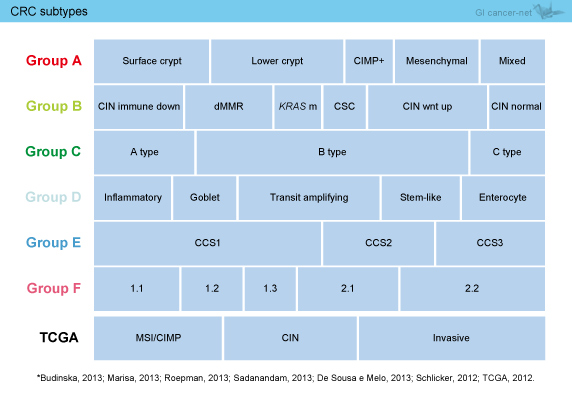
対象と方法
コンソーシアム参加の適格基準は以下に同意するものとした。
- 研究グループが有するデータを提供する
- 各グループより蓄積されたデータの統合解析を行う
- 分子サブタイプのコンセンサスを明確にする
実際に参加したグループは以下のとおりであった (表1)。各グループより集積した遺伝子発現のデータを基に、それぞれのグループが独自にサブタイピングしたサンプルについて統合解析およびクラスタリングを行い、Consensus Molecular Subtype (CMS) を決定した。
表1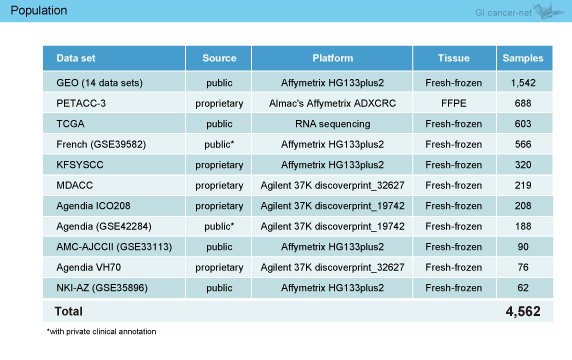
結果
集積された使用可能なデータの背景を表2に示す。
表2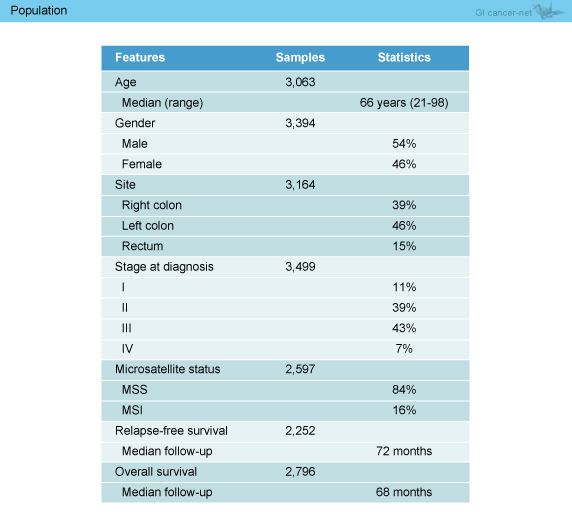
解析の結果、CMS1: 13%、CMS2: 35%、CMS3: 11%、CMS4: 20%、分類不能21%に分類された。その後、使用可能な臨床背景データを用い解析したところ、CMS1では女性・右側原発巣・マイクロサテライト不安定性 (MSI) の割合が多く、CMS4では進行期症例の割合が多かった。
また、エクソーム変異データ (使用可能な282例) との相関解析では、CMS1で変異率が高く、ゲノムコピー数変化 (copy number alterations: CNA) データ (使用可能な550例) との相関解析では、CMS1でCNAの割合が低く、CMS2, 4で高かった。BRAF、KRAS 変異 (使用可能な2,386例) との相関解析においては、CMS1でBRAF 変異率が高く、CMS3でKRAS 変異率が高かった。さらに、439例の蛋白アレイ情報と3,891例の活性化しているシグナル経路との相関解析を行ったところ、特にCMS3でIGFBP2発現が高く、CMS2でWNT経路が活性化しているのが特徴的であった。
結果のまとめを表3に示す
表3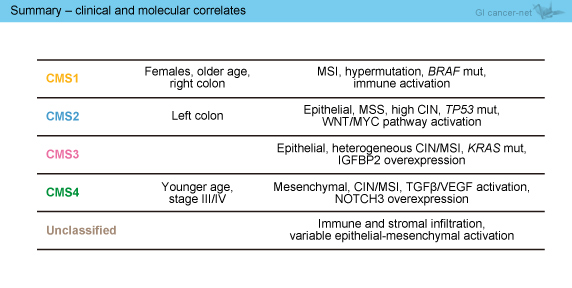
続いて臨床データとの解析を行ったところ、2,252例でのRFS (relapse-free survival) との相関解析では、CMS1が予後良好でありCMS4が不良であった (CMS4 vs. CMS1: HR=1.8, p=0.01) (図2)。
図2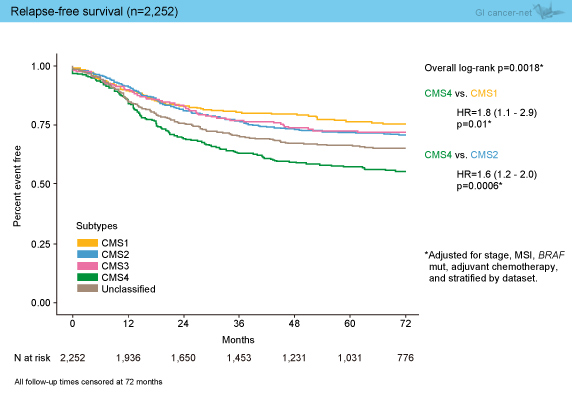
2,796例でのOSとの相関解析では、CMS2、CMS1が予後良好で、CMS4が不良であった (CMS4 vs. CMS2: HR=1.7, p=0.0004) (図3)。なお、興味深いことに、593例で再発後の予後を解析したところ、CMS2の予後が良好で、上述の解析でRFSが良好であったCMS1の予後が一番不良な結果であった (CMS1 vs. CMS2: HR=2.3, p=0.001) (図4)。
図3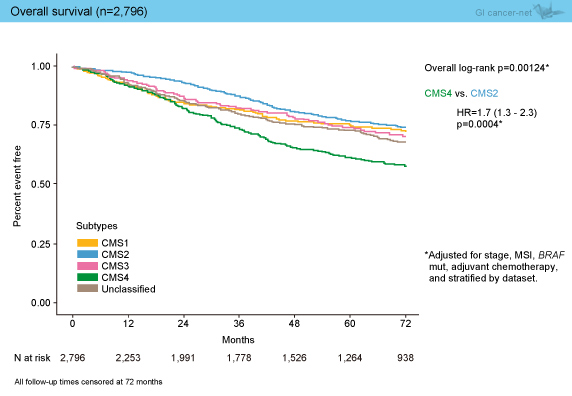
図4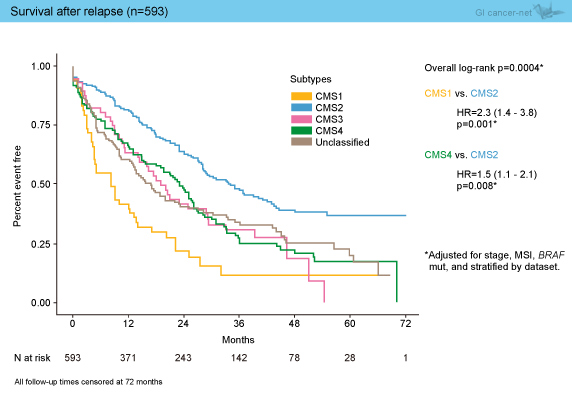
現在、このコンソーシアムによるサブタイピングはまだ進行中で、今回分類不能となった群の解析や他のデータセットによる確認が報告される予定である。さらに、効果予測因子としての評価や標的薬剤感受性判断への応用に進めていくことを検討している。
結論
CRCSCは、各研究グループの「collaboration and sharing」の精神に基づき、癌のサブタイピングに関する新しい方法論を作り上げた。大規模な大腸癌サンプルを使用して4つの生物学的なサブタイプを同定し、術後大腸癌の予後予測が可能なことを示した。
コメント
CRCSCは、さまざまなコンセプトや方法で大腸癌の分子サブタイピングを行っている名だたる各研究グループ (TCGA、MDACC、PETACC等) のデータを集結させ、共通のコンセンサスを構築し、膨大なデータからの統合解析を実施することが目的のプロジェクトである。本研究のために抽出されたデータを統合解析することにより、全体がCMS1~4、分類不能の5群に分類できた。結果は上述の如くであり、乳癌領域で臨床応用されているintrinsic subtypeに比べて、予後予測因子であるMSIに加え、現在注目されているimmune activation / infiltrationや多くのシグナル経路活性との相関が解析され、各群の予後との相関が示されていることが評価される。しかしながら、遺伝子発現解析がベースとなっているため、検体の条件や腫瘍のheterogeneity、多様な測定方法を踏まえると、臨床応用していくにはまだ問題が残されており、あくまでも「コンセンサス」であることを考慮しなければならない。
この研究の最大の結論は、トランスレーショナル研究領域においても、研究グループが集まり世界的なコンセンサスを作り上げることができた、ということであろう。今後は、分類不能群のさらなる解析等も必要であるが、各群に最適な分子標的薬を選択することも視野に入っており、CRCSCのこれからの研究発表が大いに期待される。
今回の米国臨床腫瘍学会年次集会のテーマが示すように、これまで蓄積されたエビデンスを患者さんに還元する時代になってきた。バイオマーカー研究においても決して例外ではない。これからの大腸癌診療は、術後すぐに組織検体を提出し、コンセンサスに従ったサブタイピングを調べることにより、予後改善や最良の治療薬推奨が可能となり、患者毎の適切なフォローアップ期間や、術後補助化学療法の必要性の有無、再発時の治療法の検討などができるような個別化医療を現実化していかなければならないであろう。
(レポート:砂川 優 監修・コメント:小松 嘉人)


