背景と目的
局所進行直腸癌に対して、フッ化ピリミジン系製剤を用いた術後補助化学療法は予後を改善し、術前化学放射線療法は術後化学放射線療法と比較しDFS (disease-free survival) を改善することが報告されている1)。一方、結腸癌においてはL-OHPを併用した術後補助化学療法 (FOLFOX、XELOX) が生存予後を改善することが示され、推奨されている。
ADORE試験は、これらの結果をもとにフッ化ピリミジン系製剤併用の術前化学放射線治療後にTMEを行い、病理学的診断でypStage II/IIIであった症例に対する術後補助化学療法として、L-OHP併用による上乗せ効果を検討した無作為化第II相試験である。
対象と方法
対象は、局所進行直腸癌に対してフッ化ピリミジン系製剤併用の術前化学放射線療法後にTMEが行われ、病理学的診断でypStage II (ypT3-4N0)、ypStage III (ypTanyN1-2) とされた症例で、術前にL-OHPを併用した症例は除外された。
上記症例が、FOLFOX群 (L-OHP: 85mg/m2, day1、Leucovorin: 200mg/m2, day1、bolus 5-FU: 400mg/m2, day1、infusional 5-FU: 2,400mg/m2, civ for 46hs、2週毎8サイクル)とFL群 (Leucovorin: 20mg/m2/day, day1-5、5-FU: 380mg/m2/day, day1-5、4週毎4サイクル) に、1:1で無作為に割り付けられた (図1)。
主要評価項目は3年DFSであり、FOLFOX群78%、FL群70%の仮説のもと片側α=0.05、検出力80%で、必要症例数は1群160例であった。また、副次評価項目は有害事象、再発様式、OS、QOLであった。
図1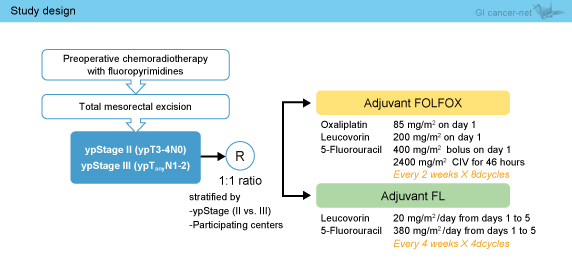
結果
2008年11月~2012年6月に321例が登録され、FOLFOX群160例、FL群161例に割り付けられたが、同意撤回などにより、実際に治療が行われたのはFOLFOX群146例、FL群149例であった。データカットオフは2013年12月で、観察期間中央値は38.2ヵ月であった。
患者背景は、すべての臨床病理学的因子で両群バランスがとれており、差を認めなかった。年齢中央値は55歳であり、すべての症例が5-FU/LV、Capecitabine、UFTのいずれかを用いた術前化学放射線療法とTMEを受けていた。なお、術後ypStage IIは両群ともに約40%であった。
両群ともに約95%の症例で予定されたサイクル数を完遂でき、治療遅延はFOLFOX群58.9%、FL群37.6%、減量はそれぞれ61.0%、31.5%であった。また、FOLFOX群における相対用量強度は、bolus 5-FU 86.6%、infusional 5-FU 87.6%、L-OHP 93.2%であり、FL群ではbolus 5-FU 95.0%であった。
主要評価項目であるITT解析によるDFSは、3年DFSがFOLFOX群71.6%、FL群62.9%であり、有意差を認めた (HR=0.630, 95% CI: 0.413-0.962, p=0.032) (図2)。
図2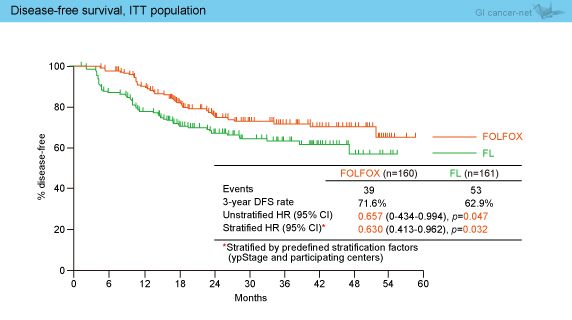
ypStage III症例における解析では、3年DFSはFOLFOX群66.6%、FL群57.3%であり、有意差を認めた (HR=0.602, 95% CI: 0.371-0.977, p=0.040)。一方、ypStage II症例の3年DFSはFOLFOX群81.6%、FL群71.3%であり、有意差を認めなかった (HR=0.744, 95% CI: 0.334-1.657, p=0.469)。
サブグループ解析のforest plotを図3に示す。多くの臨床病理学的因子においてFOLFOX群で良好な傾向にあったが、特にypT3-4、ypN1b、ypN2では有意に良好であった。また、術前化学放射線療法において効果なしまたは最小であった症例においてもFOLFOX群で有意に良好であった。これらの結果は、より進行した症例でFOLFOXが有効であることを示唆する。
図3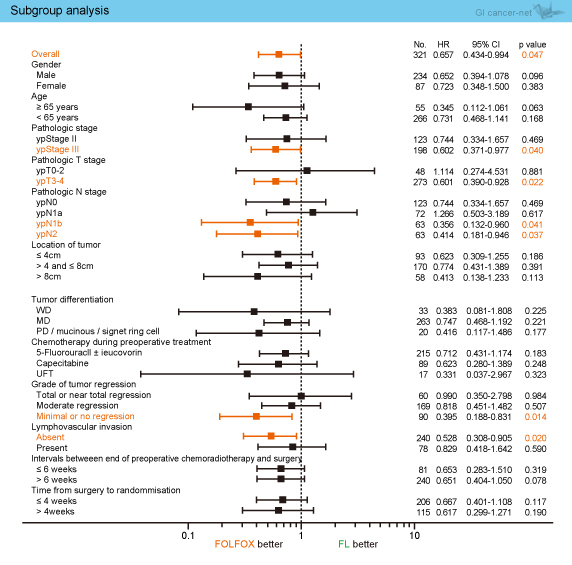
3年DFSに対する多変量解析では、FOLFOXは独立した予後因子であった (HR=0.554, p=0.008) (表1)。
表1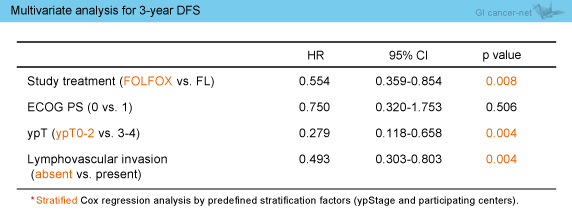
有害事象は、好中球減少、血小板減少、末梢神経障害、倦怠感、悪心の全gradeの発現率はFL群に比べてFOLFOX群で増加したが、grade 3/4の有害事象の発現率には差を認めなかった (表2)。
表2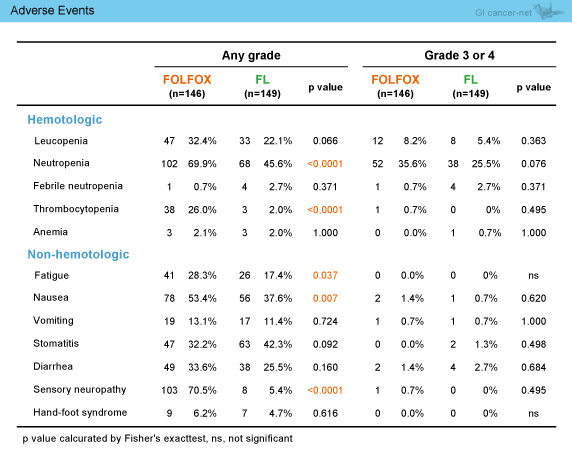
結論
ADORE試験において、術前化学放射線療法後にypStage II/IIIであった症例に対して、術後のFOLFOXはFLと比較し3年DFSを改善し、多変量解析においても有意な因子であった。また、術前化学放射線療法を受けた症例においても、術後のFOLFOXの忍容性は良好であった。OSを含めた副次評価項目の検討のため、さらなるフォローアップが必要である。
コメント
直腸癌に対する術後の補助化学療法に焦点を絞った検討である。術前にフッ化ピリミジン系製剤を用いた化学放射線療法を行い、TMEを施行してypStage II、ypStage IIIと診断された症例を対象に、術後補助化学療法としてFOLFOXとFLの比較がなされたが、FOLFOX群の3年DFSが有意に良好であった。L-OHP未使用の化学放射線療法による効果が希薄な症例を対象としたため、術後補助化学療法におけるL-OHPの上乗せ効果が明らかになったものと考えられる。なお、直腸癌に対する術前化学放射線療法においてL-OHPを併用しなくてはならないエビデンスはないため (#3500、#3501、#3603参照)、L-OHPを併用しない術前補助療法を施行することには妥当性がある。
大腸癌の化学療法においてL-OHPの併用効果が期待できる症例を選択する意義は大きい。MSIの有無や大腸癌の分子生物学的なsubtypingなどによって、大腸癌の悪性度、ひいては術後補助化学療法の必要性を判定する試みがなされている。さらに術前補助療法を施行した直腸癌では、切除標本の病理組織学的所見から抗癌剤への感受性を類推できる。貴重な切除標本から得られる情報は、余すところなく利用したいものである。
(レポート:中村 将人 監修・コメント:大村 健二)
- Reference
-
- 1) Rödel C, et al.: J Clin Oncol. 25(1): 110-117, 2007[PubMed]


