Abstract #3511
切除不能進行・再発大腸癌初回治療例に対するCetuximab併用療法におけるKRAS G13D変異*の影響
*KRAS codon13のグリシンからアスパラギン酸への変異 (G13D)
Influence of KRAS G13D mutations on outcome in patients with metastatic colorectal cancer (mCRC) treated with first-line chemotherapy with or without cetuximab.
Sabine Tejpar, et al.

切除不能進行・再発大腸癌に対するCetuximab療法はKRAS 野生型においてのみ有効とされ、変異型に対しては無効とされているが、さまざまなKRAS 変異を同様に扱ってよいか否かは不明である。大腸癌では肺癌や膵癌と比較してcodon13変異が多いこと、in vitroの検討ではcodon13変異における形質転換活性がcodon12変異よりも弱いこと、cell lineにおける検討ではKRAS G12V変異細胞株に対してCetuximabは無効であるが、G13D変異細胞株に対しては有効であることが報告されている。
さらに、切除不能進行・再発大腸癌既治療例における後ろ向き解析において、KRAS G13D変異を有する症例は予後不良であり、Cetuximabを含む治療によりPFS (progression-free survival) やOS (overall survival) が延長する傾向が認められたと報告されている1)。今回、切除不能進行・再発大腸癌初回治療例に対するCetuximab併用療法におけるKRAS G13D変異の影響を検討した。
さらに、切除不能進行・再発大腸癌既治療例における後ろ向き解析において、KRAS G13D変異を有する症例は予後不良であり、Cetuximabを含む治療によりPFS (progression-free survival) やOS (overall survival) が延長する傾向が認められたと報告されている1)。今回、切除不能進行・再発大腸癌初回治療例に対するCetuximab併用療法におけるKRAS G13D変異の影響を検討した。
CRYSTAL試験 (第III相; FOLFIRI vs. FOLFIRI + Cetuximab)、OPUS試験 (第II相; FOLFOX4 vs. FOLFOX4 + Cetuximab) に登録された症例を対象に、KRAS 野生型、KRAS G13D変異型、KRAS G12V変異型、KRAS 変異型 (G13D、G12V以外) におけるPFSおよびOS、RR (response rate)を比較・検討した。
KRAS 野生型におけるCetuximab非併用群は447例、併用群は398例、KRAS G13D変異型では各41例、42例、KRAS 変異型 (G13D以外) では各201例、249例であり、性別、年齢、PS、転移臓器などの患者背景に大きな隔たりはなかった。
Cetuximab非併用群におけるPFSはKRAS 野生型で7.6ヵ月、KRAS G13D変異型で6.0ヵ月、KRAS G12V変異型で8.8ヵ月、KRAS 変異型 (G13D、G12V以外) で8.1ヵ月、OSは各19.5ヵ月、14.7ヵ月、17.8ヵ月、17.7ヵ月、KRAS G13D変異型とその他のKRAS 変異型との比較ではPFSのハザード比が1.54 (p=0.0847)、OSのハザード比が 1.39 (p=0.0988) と、有意差は認めないもののKRAS G13D変異型で不良であった。
PFS (併用群 vs. 非併用群) のハザード比はKRAS 野生型で0.66、KRAS G13D変異型で0.60、KRAS G12V変異型で1.55、KRAS 変異型 (G13D、G12V以外) で1.37、OSのハザード比は各0.81、0.80、1.10、1.16、RRのオッズ比は各2.17、2.41、0.54、0.58 と、KRAS G13D変異型ではKRAS 野生型と同様の傾向を認め、Cetuximabの有効性が示唆された。
Cetuximab非併用群におけるPFSはKRAS 野生型で7.6ヵ月、KRAS G13D変異型で6.0ヵ月、KRAS G12V変異型で8.8ヵ月、KRAS 変異型 (G13D、G12V以外) で8.1ヵ月、OSは各19.5ヵ月、14.7ヵ月、17.8ヵ月、17.7ヵ月、KRAS G13D変異型とその他のKRAS 変異型との比較ではPFSのハザード比が1.54 (p=0.0847)、OSのハザード比が 1.39 (p=0.0988) と、有意差は認めないもののKRAS G13D変異型で不良であった。
PFS (併用群 vs. 非併用群) のハザード比はKRAS 野生型で0.66、KRAS G13D変異型で0.60、KRAS G12V変異型で1.55、KRAS 変異型 (G13D、G12V以外) で1.37、OSのハザード比は各0.81、0.80、1.10、1.16、RRのオッズ比は各2.17、2.41、0.54、0.58 と、KRAS G13D変異型ではKRAS 野生型と同様の傾向を認め、Cetuximabの有効性が示唆された。
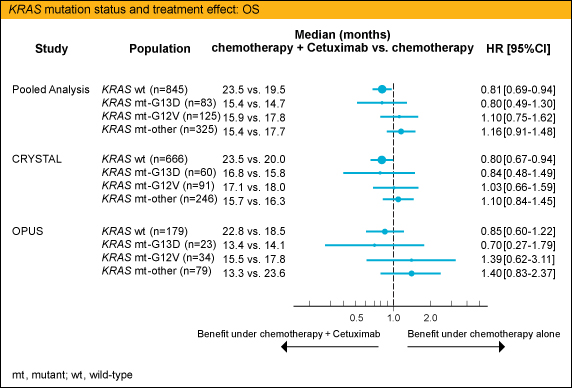
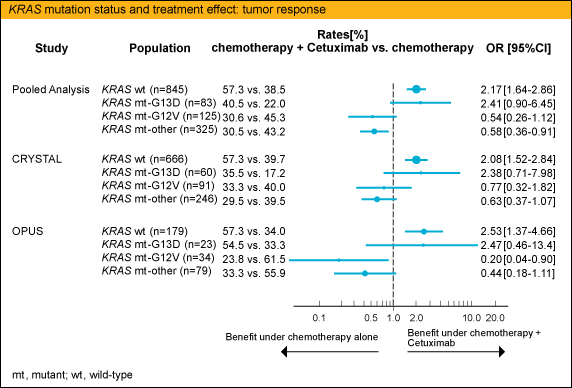
Cetuximabの治療効果はKRAS 遺伝子の変異の部位により異なることがCRYSTAL試験、OPUS試験においても確認された。KRAS G13D変異を有する切除不能進行・再発大腸癌初回治療例の予後は不良であったが、他のKRAS 変異型とは異なり、KRAS 野生型と同様のCetuximabの上乗せ効果が示唆された。
大腸癌におけるKRAS の変異は約40%の症例に認められ、そのうち約8割がcodon12の変異で、約2割がcodon13の変異であり、その他の部位の変異は数%と極めて少ないことが報告されている。Codon13の変異はそのほとんどがG13Dである。今回の米国臨床腫瘍学会年次集会では、我が国からもG13D変異型に関する発表がなされていたが、その頻度はKRAS 変異型全体の19.5%であり、人種差はないものと思われる(Abstract #3605)。KRAS 変異型は、部位により生物学的意義が異なることが指摘されており、codon13の変異、特にG13Dにおいては予後が不良である一方、Cetuximabに対する感受性が保持されていることが報告されている。
そこで、今回CRYSTAL試験とOPUS試験の症例におけるKRAS G13D変異の意義について検討がなされた。その結果、G13D変異型においては確かにCetuximabの上乗せ効果が認められたが、化学療法単独群のRR22%、PFS中央値6.0ヵ月、MST14.7ヵ月といずれもKRAS 野生型やcodon13以外の変異型の症例に比べ著しく不良であり、生物学的悪性度が高いことや、化学療法そのものの効果に乏しいことが示唆された。
症例数が少ないため、比較試験による検証は困難と思われるが、今後の抗EGFR抗体薬の試験においてG13D変異型の症例も対象とし、前向きに検証して行く必要があるものと思われた。
そこで、今回CRYSTAL試験とOPUS試験の症例におけるKRAS G13D変異の意義について検討がなされた。その結果、G13D変異型においては確かにCetuximabの上乗せ効果が認められたが、化学療法単独群のRR22%、PFS中央値6.0ヵ月、MST14.7ヵ月といずれもKRAS 野生型やcodon13以外の変異型の症例に比べ著しく不良であり、生物学的悪性度が高いことや、化学療法そのものの効果に乏しいことが示唆された。
症例数が少ないため、比較試験による検証は困難と思われるが、今後の抗EGFR抗体薬の試験においてG13D変異型の症例も対象とし、前向きに検証して行く必要があるものと思われた。
(レポート:山﨑 健太郎 監修・コメント:寺島 雅典)

このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。