Abstract #4085 |
転移を有する大腸癌に対する一次治療としてのpanitumumab+FOLFIRI併用療法の第II相試験(20060314)の最新解析 |
Updated Analysis of a Phase II Study (20060314) of Panitumumab with FOLFIRI as First-Line Treatment of Patients with Metastatic Colorectal Cancer. |
|
完全ヒト型抗EGFR抗体であるpanitumumab(pmab)は、化学療法抵抗性の転移を有する大腸癌に有効性が示されている。最近、KRAS変異の有無によって、転移を有する大腸癌に対する抗EGFR抗体治療の効果が予測可能であるとのデータが多数報告されている。本報告は、一次治療としてのpmab+FOLFIRI併用療法の有効性とKRASとの関連をプロスペクティブに評価した、オープンラベル単アーム多施設共同第II相試験(20060314)の中間解析である。
対象は、欧州36施設より登録された、組織学的に転移を有する大腸癌と確認され、過去に全身的治療を受けていないPS0-2の症例である。
pmab 6mg/kg+FOLFIRIを2週に1回投与した。pmabはFOLFIRIの前に1時間かけて点滴投与し、初回投与時に忍容性が認められた場合、2回目以降は30分間で投与した。
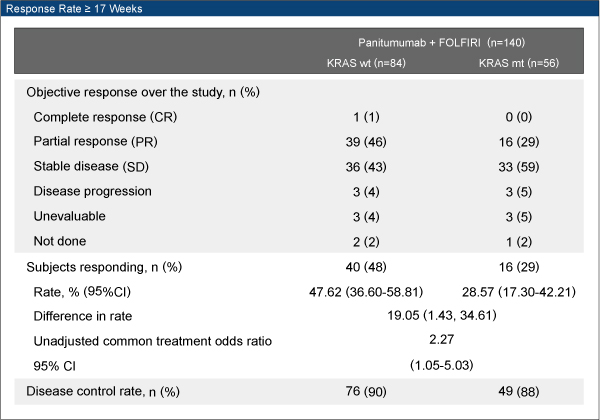
一次エンドポイントはobjective response rate(ORR)、二次エンドポイントはdisease control rate、PFSを含む有効性と安全性とし、KRAS遺伝子変異の有無による評価を行った。
154例が登録され、147例の腫瘍切片標本について検査が可能であった。そのうち、KRASの遺伝子型が確認された142例(KRAS野生型:60%、KRAS変異型:40%)を解析対象とした。
全症例のORRは41%、KRAS遺伝子型の解析ではKRAS野生型が48%、KRAS変異型が29%であり、KRAS野生型においてより高い有効性を示した(OR=2.27、95%CI:1.05-5.03)。
有害事象は下表の通りである。KRAS遺伝子変異の有無は、有害事象の発生頻度に影響を与えなかった。
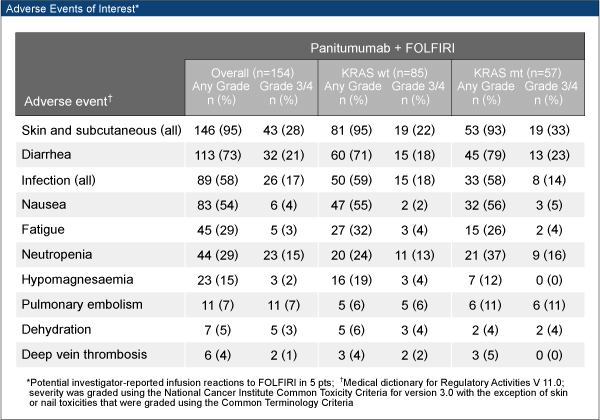
また、治療に関連する死亡は3例報告された。(KRAS野生型:吐血、直腸出血、KRAS変異型:大静脈血栓症)。
本試験は、一次治療としてのpmab+FOLFIRI併用療法におけるKRAS遺伝子変異の有無と治療の効果を検討した初のプロスペクティブな解析である。この中間解析により、pmab+FOLFIRI併用療法は有効で忍容性が高いことが確認された。このほか、現在pmabは一次療法としてのFOLFOXとの併用療法を検討する第III相試験(20050203)が進行中である。
完全ヒト型抗EGFR抗体panitumumabの進行・再発大腸癌に対する有用性を検証する臨床試験が多角的に進められている。cetuximabに関する同様の検討が先行して行われたため、途中まで道が示されていることが迅速な進行を可能にしている。本試験は第II相試験であるが、KRAS遺伝子変異の頻度を考慮して登録症例数が150例に設定されたものと思われる。結果は極めて妥当なものであり、抗EGFR抗体療法におけるKRAS遺伝子変異の有無の意義が再確認された。なお、皮疹も含めた有害事象の発生頻度、およびその程度とKRAS遺伝子変異の有無との間に関連は認められていない。これらのことは、KRASが野生型でかつ皮疹が高度な症例が最もlong survivorである可能性を示していると考えられる。
(コメント・監修:大村 健二)