ケースカンファレンス~トップオンコロジストはこう考える~
監修中島 貴子 先生聖マリアンナ医科大学
臨床腫瘍学
日常診療で遭遇する症例を取りあげ、トップオンコロジストが治療方針を議論するケースカンファレンスをお届けします。
CASE6
2017年10月開催
PS不良の大腸癌多発肝転移例
に対する治療戦略
 牧山 明資 先生
牧山 明資 先生
JCHO 九州病院
血液・腫瘍内科 加藤 健 先生
加藤 健 先生
国立がん研究センター
中央病院 消化管内科
 小髙 雅人 先生
小髙 雅人 先生
医療法人薫風会 佐野病院
消化器がんセンター 坂井 大介 先生
坂井 大介 先生
大阪大学大学院
医学系研究科 先進癌薬物療法開発学寄附講座
- 症例プロファイル①
- ディスカッション 1
PS不良の盲腸癌
多発肝転移に対する治療 - ディスカッション 2
盲腸癌切除後の多発肝転移
増悪に対する治療 - 症例プロファイル②
- ディスカッション 3
黄疸を伴うPS不良の大腸癌多発肝転移の治療方針 - まとめ
ディスカッション 2 盲腸癌切除後の多発肝転移増悪に対する治療
盲腸原発巣切除後の多発肝転移増悪に対する治療をどのように進めるか?
牧山この症例に対する実際の治療ですが、サブイレウスと考え原発巣の切除が先に行われました。ところが、術後2週間で肝胆道系酵素が上昇し、18日目に化学療法目的で当科に紹介となりました。この時点で、すでにPSは2で、上腹部の疼痛と腹部膨満、下肢の浮腫を認めました。
紹介時のデータを提示します(図3)。白血球数が増加し、PT-INRも1.2と延長傾向を示しました。ビリルビン値が上昇しており、トランスアミナーゼ、ALP、γ-GTPも上昇しました。そのほかにも低ナトリウム血症、軽度の高カリウム血症があり、CRPが10 mg/dLと高度の炎症も認められました。腫瘍マーカーもさらに上昇していました。
CT検査では、術前に比べて術後には、加藤先生が懸念されたように、肝転移巣がかなり増大した状況で、腹水も増えていました(図4)。肺転移巣も新たに出現し、RAS遺伝子型は検査結果待ちの状態です。
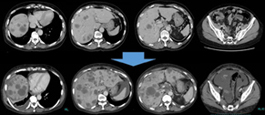 (図4)CT所見(術前→術後)
(図4)CT所見(術前→術後)
- 両肺に小結節が複数出現。肝両葉に多数の低吸収腫瘤認め腫大あり。
- 肝門部、大動脈周囲にリンパ節腫大。腹水多量。
牧山多量の腹水と、肝胆道系酵素の上昇を伴うこの患者さんの治療方針について、先生方のお考えをお聞かせください。
加藤術後早期に肝転移巣が急激に増殖してきたわけですから、治療のチャンスは1回きりと考えて、FOLFOXをベースとした治療を選択します。術後早期なのでBevacizumabは使用しにくい、Irinotecanも肝機能への影響を考えると使いにくいので、懸案はFOLFOXに抗EGFR抗体を併用するかどうかです。RAS野生型かどうか分かりませんが、化学療法に何かをプラスして最大限できることは何かと考えると、FOLFOX+抗EGFR抗体も検討したいと思います。右側病変例なので、抗EGFR抗体の有効性は限定的かもしれませんが。
牧山坂井先生はいかがでしょうか。

坂井この症例はいわゆるESMO consensus guidelines1)におけるcytoreduction、disease controlのどちらを目指すのかという観点からは、症状も出ていますし急速な病状の進行もみられますので、誰がみてもcytoreductionを目指すことになると思います。fitかunfitかという観点からは少し悩ましいところがありますが、まだお若いですし、まずは少なくとも化学療法2剤併用療法は行いたいと思います。黄疸が出ておりIrinotecanは使用できませんので、3剤併用療法はリスクが高く、やはり2剤併用の化学療法のベースはOxaliplatinベースのFOLFOXになります。術後18日という状況を考えると、創傷治癒遅延の観点からBevacizumabも初回導入時には使用しにくいです。また、RAS変異型だった場合には、抗EGFR抗体が腫瘍を増悪させるリスクもありますので初回導入時のRAS遺伝子検査の結果が出ていない時点での使用は好ましくないと考えます。そのためFOLFOXで開始して、RAS遺伝子検査の結果を待つ、もしくは術後1ヵ月半が経過するのを待ってからBevacizumabを併用するのもよいかと思います。
牧山小髙先生、ご意見をお願いします。
小髙64歳という年齢を考えても化学療法は行うと思います。OxaliplatinかIrinotecanかという選択は、黄疸があることを考えると、Irinotecanではなく、Oxaliplatinを選択します。分子標的薬については、Bevacizumabは術後17日目では使用できませんし、抗EGFR抗体薬もRAS遺伝子検査の結果を待たないと投与できませんから、とりあえずはFOLFOXかXELOXが選択肢になりますが、将来抗EGFR抗体薬を使用することになったときのことを考えると、FOLFOXを選択して、RAS遺伝子検査の結果を待って、野生型であれば右側ですが抗EGFR抗体薬を併用します。変異型であれば術後4週間が経過した後にBevacizumabを併用します。
牧山皆さん、RAS遺伝子検査の結果を待って、抗EGFR抗体薬とBevacizumabを使い分けるという方針で意見が一致しましたね。ところで、Irinotecanが使用できる状況(総ビリルビン 1.5 mg/dL以下でAST・ALT 100 U/L以下、肝転移があれば200 U/L以下等)であれば、右側の大腸癌でcytoreductionを要する症例と言うことでFOLFOXIRI+Bevacizumabも検討されますでしょうか。
加藤アグレッシブな病勢を考えた場合、使用する方向で検討します。
小髙PS 2でも、検討するのでしょうか。
牧山この症例は痛みが強いのでPS 2としましたが、痛みが消失したらPSは1と考えてよいと思います。小髙先生、ストーマ造設、バイパス術施行後、2週間でBevacizumabの併用を開始しますか。
小髙ストーマ造設後は1週間後であってもBevacizumabの併用を開始しますが、バイパス術では吻合しますから、Bevacizumabの併用を開始するのは4週以降です。ただし、バイパス術も腹腔鏡下で行えば、2週間後には化学療法を開始できると思います。
その後の治療経過と手術を先行させた場合の可能性

牧山この患者さんは化学療法としてFOLFOXを選択しました。抗腫瘍効果が得られず、全身状態が悪化するだけのケースもありますから、患者さんには十分にインフォームド・コンセントを行いました。若年ということもあり、患者さんは治療を希望されました。肝機能障害も黄疸も出ているので、治療は急いだほうがよいということで、ポートの作成のために手術室が空くのを待たずに、末梢静脈からFOLFOX療法を行いました。数日後にRAS野生型であることが判明し、実はこの当時はsidenessの考え方がなかったため、迷わずPanitumumabを併用しました。しかしながら、効果は認められず、肝胆道系酵素も徐々に上昇し、さらには播種性血管内凝固症候群(DIC)まで発症し、全身状態が悪化したため、化学療法もPanitumumabも1コースしか投与できず、肝不全、腎不全が進行し、治療開始から1ヵ月ほどで腫瘍進行に伴う原病死という転帰を辿られました。振り返ると、RASは野生型でしたが、右側ということもありBRAF変異の可能性もあったと思いますが、結果的に抗EGFR抗体薬が効きにくい癌だったのかもしれません。
坂井この症例は、手術を先行させずに化学療法を先行させたら、どうなったと思われますか。
加藤かなり効いた可能性がありますよね。
小髙切除したから化学療法が効いたという方もいますし、切除が腫瘍増大のきっかけになる方もいます。結果論ですが、この方は化学療法を先行させたほうがよかったように思います。
坂井しかし、やってみないと結果は分かりませんからね。
加藤狭窄を解除することだけが目的であれば、例えばストーマを造設して、早期に化学療法を開始するという選択肢もあったかもしれません。
小髙この症例はストーマを造設するとしたら、小腸ストーマになるので、下痢が生じて、化学療法は行いにくくなるように感じます。
加藤下痢はアヘンチンキなどでコントロールしつつ、バイパス術も含めて、なるべく早期に化学療法を開始できるような状況にするのが、よかったように思います。
牧山なるほど。ありがとうございます。こうした症例では内科と外科が相談して、消化管狭窄に対応、早期に適切な化学療法を選択・開始できるようにすることが重要だと思います。
全身状態不良例に対する化学療法の報告
牧山PS不良例に対する化学療法については設樂先生が報告されていますが、PS不良、高度な腫瘍関連合併症を有する8例に対して、FOLFOX+Cetuximabを投与し、6例では病状の改善が認められました2)。全例がKRAS野生型、2例がBRAF変異型でした。この検討が行われた当時はsidenessの考え方はなく、原発部位については記載がありません。CT画像からは、肝転移巣や腹水などが改善していることが分かります。
GI cancer-net
消化器癌治療の広場

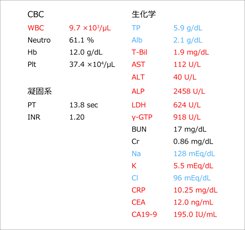 (図3)外科から内科への紹介時の血液検査
(図3)外科から内科への紹介時の血液検査