START試験[S-1 + Docetaxel(DOC) vs. S-1]のUpdate reportである。この演題はESMOのCongress highlightsのトップにも取り上げられた。
今回のupdate reportでは主要評価項目であるS-1 + DOC のS-1に対するOS (overall survival)の有意差が報告された。生存期間中央値が12.5ヵ月 vs. 10.8ヵ月、17%のリスク軽減効果が得られ、PFS (progression-free survival) などでも有意に良好な結果であり、発表者の吉田教授は「S-1 + DOC療法が胃癌の標準治療のひとつとなる」と強調した。
しかしながら以前2011年 消化器癌シンポジウムでのprimary analysisで「有意差が認められていない」と報告されていたことが、今回のディスカッションでもディスカッサントのDouillard先生に指摘され、これにより評価が分かれることとなった。ただ、試験成績、有害事象プロファイルなども良好であること、欧米での今後のDCF (DOC + Cisplation + 5-FU) 療法などのDOCの用量にも影響を与える可能性などのポイントについても言及していた。
本試験は、プラチナ以外の薬剤との併用療法としてのみならず、胃癌でよく経験される標的病変のない癌性腹膜炎に対する治療法として高い有用性を示したことは間違いない。
いずれにせよ、胃癌は日本が中心となり情報発信を行わねばならない癌であり、今回本試験により日本からまた新たな胃癌化学療法が発信されたことは喜ばしいことである。
今後S-1 + DOC療法に対し、癌性腹膜炎症例やプラチナ併用しにくい患者を中心としての臨床応用や今後の補助化学療法などの臨床試験の試験治療群としてのさらなる評価が待たれる。
本試験の結果は、既に2011年 消化器癌シンポジウムで報告されており、主要評価項目であるOSはS-1 + DOC群390日、S-1群334日と有意差は認められなかった (HR=0.88, 95%CI: 0.735-1.044, p=0.1416)。しかし、多数のcensored caseが解析時のイベント数不足につながっていることが、独立した生物統計学者により指摘された。
そこで、censored caseの問題を解決するために、今回、OS 619例 (97.5%) とPFS 616例 (97.0%) のイベント発生が確認された時点での解析を行った。観察期間中央値は11.4ヵ月であった。
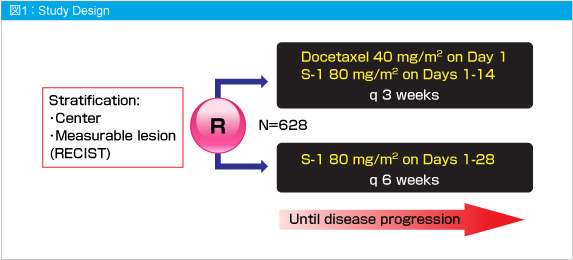
試験デザインを図1に示す。主要評価項目はOSであり、副次評価項目はPFS、RR、安全性であった。
対象は、RECIST version1.0により測定可能病変または測定不能病変を有すると判定された切除不能な進行または再発胃癌 (胃・食道接合部腺癌を含む) で、年齢は20-79歳、経口摂取可能、PS≦1、未治療例であった。
2005年9月から2008年9月の間に639例が登録され、ITT解析対象となったのは635例 (S-1 + DOC群314例, S-1群321例) であった。両群の患者背景に偏りはみられず、平均治療コースは、S-1 + DOC群6.1コース (18.3週)、S-1群3.3コース (19.8週)であった。
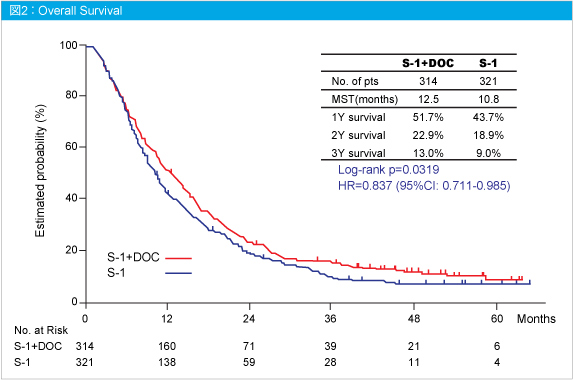
主要評価項目であるOSは、S-1 + DOC群で12.5ヵ月、S-1群で10.8ヵ月であり、S-1 + DOC群おいて有意な延長が認められた (HR=0.837, 95%CI: 0.711-0.985, p=0.0319) (図2)。
副次評価項目であるPFSは、S-1 + DOC群で5.3ヵ月、S-1群で4.2ヵ月であり、S-1 + DOC群おいて有意な延長が認められた (p=0.001)。測定可能病変例 (n=480) に対するRRはS-1 + DOC群38.8%、S-1群26.8%と、有意にS-1 + DOC群で高かった (p=0.005)。
安全性においては、grade 3以上の白血球減少、好中球減少、発熱性好中球減少の発現率がS-1群に比べS-1 + DOC群で高かったが、忍容可能であった。
なお、事前に層別された測定病変別の解析では、測定可能病変例におけるPFSはS-1 + DOC群4.7ヵ月、S-1群3.9ヵ月と、S-1 + DOC群で有意に延長がみられたのに対し (HR=0.822, 95%CI: 0.686-0.985, p=0.0324) 、OSはS-1 + DOC群11.7ヵ月、S-1群10.3ヵ月と有意差は認められなかった (HR=0.904, 95%CI: 0.751-1.088, p=0.2849) 。一方、測定不能病変例におけるPFSはS-1 + DOC群8.4ヵ月、S-1群5.6ヵ月 (HR=0.613, 95%CI: 0.435-0.862, p=0.0045) 、OSはS-1 + DOC群17.9ヵ月、S-1群12.0ヵ月 (HR=0.649, 95%CI: 0.461-0.914, p=0.0127) と、いずれもS-1 + DOC群で有意に延長した。
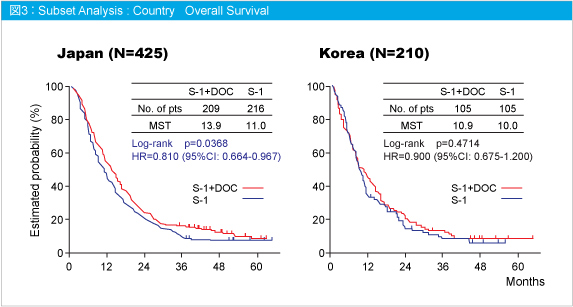
また、国別のサブセット解析においては、日本人のOSはS-1 + DOC群で有意な延長を示したが (HR=0.810, p=0.0368) 、韓国人では有意差が認められなかった (HR=0.900, p=0.4714) (図3)。