2011年9月23日~27日にスウェーデン・ストックホルムにて開催されたThe European Multidisciplinary Cancer Congress 2011 - ESMOより、大腸癌や胃癌などの注目演題のレポートをお届けします。演題レポートの冒頭には、臨床研究の第一線で活躍する監修ドクターのコメントを掲載しています。

化学療法不応の切除不能進行・再発大腸癌患者に対するTAS-102 + BSC療法の多施設共同無作為化二重盲検比較第II相試験:主要結果と効果予測バイオマーカー (TK1およびTP発現) に関する報告
#6005
A Multicenter, Randomized, Double-Blind, PhaseⅡof TAS-102 (A) plus Best Supportive care (BSC) Versus Placebo (P) Plus BSC in Patients (pts) With Chemo-therapy refractory Metastatic Colorectal Cancer (mCRC)
A Multicenter, Randomized, Double-Blind, PhaseⅡof TAS-102 (A) plus Best Supportive care (BSC) Versus Placebo (P) Plus BSC in Patients (pts) With Chemo-therapy refractory Metastatic Colorectal Cancer (mCRC)
Yasutoshi Kuboki, et al.

#6099
The Value of Thymidine Kinase 1 (TK1) and Thymidine Phosphorylase (TP) Expression as Predictive Factors With the Treatment Efficacy of TAS-102, a Novel Antitumor Agent, in Patients (pts) With Metastatic Colorectal Cancer (mCRC)
Yoshito Komatsu, et al.

サルベージライン大腸癌化学療法における期待の新規代謝拮抗剤TAS-102

フッ化ピリミジン、CPT-11、Oxaliplatinが無効のKRAS 変異型やサルベージラインにおける抗EGFR抗体薬 (KRAS 野生型) の無効症例においては、有効な薬剤がないのが現状である。しかし、PS良好で化学療法の適応となる症例は少なからず存在し、有効な新規薬剤が切望されている。そのような患者対象に対して、TAS-102は主要評価項目のoverall survivalにおいてHR0.56と予後を改善させるpromisingなデータを示しており、非常に期待が持てる。
TAS-102の主な毒性は血液毒性であるが、発熱性好中球減少症も4%台であり、QOLを損なう非血液毒性である倦怠感、下痢、吐き気は認めるもののGrade 3/4の頻度は少なく忍容性は良好であり、サルベージラインで用いる薬剤としては使用しやすいと考えられる。 残念ながら今回の検討 (#6099) ではTKIやTPは有効な効果予測のバイオマーカーにはならなかったが、主試験のサブ解析 (#6005) ではKRAS 変異型の症例により効果を示すなど、興味深いデータも示されている。今後行われるであろう第III相試験で主要な結果が再現されるとともに、本剤が有効な症例を選択するバイオマーカーが示されることが切に望まれる。
TAS-102は、トリフルオロチミジン (trifluorothymidine: FTD) とその分解を阻害するチミジンホスホリラーゼ (thymidine phosphorylase: TP) 阻害剤を1対0.5の比率で配合した経口の新規ヌクレオシド系抗悪性腫瘍剤である。チミジル酸合成酵素 (thymidylate synthase: TS) 阻害に加えて、TK1 (thymidine kinase 1) によるリン酸化によりDNAに取り込まれることで、TS阻害とは別のメカニズムで抗腫瘍効果を発揮する。
切除不能進行・再発大腸癌患者18例を含む進行固形癌患者21例を対象にした第I相試験において、本剤の推奨用量は70mg/m2/day、disease control rate (DCR) は52.4%であることが示された。本試験は切除不能進行・再発大腸癌の標準化学療法に不応であった患者を対象に、TAS-102の有効性と安全性を評価した無作為化比較第II相試験である。
今回は主要結果 (#6005) とTAS-102の効果予測因子としてのTK1およびTPの発現レベルの解析結果 (#6099) を報告する。
切除不能進行・再発大腸癌患者18例を含む進行固形癌患者21例を対象にした第I相試験において、本剤の推奨用量は70mg/m2/day、disease control rate (DCR) は52.4%であることが示された。本試験は切除不能進行・再発大腸癌の標準化学療法に不応であった患者を対象に、TAS-102の有効性と安全性を評価した無作為化比較第II相試験である。
今回は主要結果 (#6005) とTAS-102の効果予測因子としてのTK1およびTPの発現レベルの解析結果 (#6099) を報告する。
Fluoropyrimidine、Irinotecan (CPT-11)、Oxaliplatin (L-OHP) を含む2レジメン以上の治療歴のある切除不能進行・再発大腸癌患者を対象として、TAS-102 + BSC群 (以下TAS-102群) とplacebo + BSC群 (以下placebo群) に2:1の割合で無作為に割り付けた。TAS-102 (70mg/m2/day) は1日2回、day 1-5とday 8-12に投与し、4週を1サイクルとして繰り返した。
主要評価項目はoverall survival (OS)、副次的評価項目はprogression-free survival (PFS)、response rate (RR)、DCR、KRAS 変異の有無による有効性とした。
免疫組織化学染色 (Immunohistochemistry: IHC) はセントラルラボにて実施した。TK1とTPの細胞質内発現は2名の病理学者が盲検下で測定し、各種発現レベルと有効性との関係性を評価した。
主要評価項目はoverall survival (OS)、副次的評価項目はprogression-free survival (PFS)、response rate (RR)、DCR、KRAS 変異の有無による有効性とした。
免疫組織化学染色 (Immunohistochemistry: IHC) はセントラルラボにて実施した。TK1とTPの細胞質内発現は2名の病理学者が盲検下で測定し、各種発現レベルと有効性との関係性を評価した。
2009年8月から2010年4月までに172例が登録され、169例で評価可能であった (TAS-102群: 112例、placebo群: 57例)。
■主要結果 (#6005)
両群間の患者背景に有意な差はみられなかった。前治療は3レジメン以上がTAS-102群で84.8%、placebo群では77.2%であり、両群ともL-OHP、CPT-11レジメンの治療歴は100%であった。Bevacizumabの使用歴はTAS-102群で77.7%、placebo群は82.5%、抗EGFR抗体薬は各々63.4%、63.2%であった。
OSの中央値はTAS-102群が9.0ヵ月、placebo群は6.6ヵ月 (HR=0.56, 95% CI: 0.39-0.81, p=0.0011) であり、TAS-102群でOSが有意に延長した (図1)。
■主要結果 (#6005)
両群間の患者背景に有意な差はみられなかった。前治療は3レジメン以上がTAS-102群で84.8%、placebo群では77.2%であり、両群ともL-OHP、CPT-11レジメンの治療歴は100%であった。Bevacizumabの使用歴はTAS-102群で77.7%、placebo群は82.5%、抗EGFR抗体薬は各々63.4%、63.2%であった。
OSの中央値はTAS-102群が9.0ヵ月、placebo群は6.6ヵ月 (HR=0.56, 95% CI: 0.39-0.81, p=0.0011) であり、TAS-102群でOSが有意に延長した (図1)。
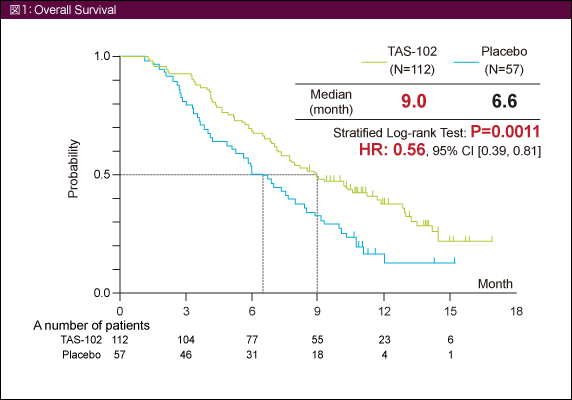
PFSの中央値はTAS-102群が2.0ヵ月、placebo群が1.0ヵ月 (HR=0.41, 95% CI: 0.28-0.59, p<0.0001)、DCRはTAS-102群43.8%、placebo群10.5% (p<0.0001)、RRは各々0.9%、0.0%であった。
TAS-102群におけるGrade3/4の主な有害事象は好中球数減少50.4%、白血球数減少28.3%、倦怠感6.2%、下痢6.2%、悪心4.4%、発熱性好中球減少症4.4%であり、治療関連死はみられなかった。
KRAS statusは149例で確認可能であり、KRAS 野生型および変異型の比率はTAS-102群で54例 (54.5%) / 45例 (45.5%)、placebo群で24例 (48.0%) / 26例 (52.0%) であった。
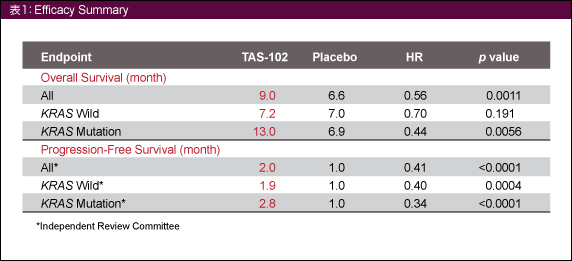
KRAS 野生型におけるOS の中央値はTAS-102群が7.2ヵ月、placebo群が7.0 ヵ月 (HR=0.70, 95% CI: 0.41-1.20, p=0.191) であり、TAS-102群の優位性は認められなかった (表1)。一方、KRAS 変異型においてはTAS-102群が13.0ヵ月、placebo群が6.9ヵ月 (HR=0.44, 95% CI: 0.25-0.80, p=0.0056) と統計学的な有意差を示した。PFSはKRAS 野生型 (p=0.0004)、変異型 (p<0.0001) ともにTAS-102群で有意に優れていた。
TAS-102群におけるGrade3/4の主な有害事象は好中球数減少50.4%、白血球数減少28.3%、倦怠感6.2%、下痢6.2%、悪心4.4%、発熱性好中球減少症4.4%であり、治療関連死はみられなかった。
KRAS statusは149例で確認可能であり、KRAS 野生型および変異型の比率はTAS-102群で54例 (54.5%) / 45例 (45.5%)、placebo群で24例 (48.0%) / 26例 (52.0%) であった。
KRAS 野生型におけるOS の中央値はTAS-102群が7.2ヵ月、placebo群が7.0 ヵ月 (HR=0.70, 95% CI: 0.41-1.20, p=0.191) であり、TAS-102群の優位性は認められなかった (表1)。一方、KRAS 変異型においてはTAS-102群が13.0ヵ月、placebo群が6.9ヵ月 (HR=0.44, 95% CI: 0.25-0.80, p=0.0056) と統計学的な有意差を示した。PFSはKRAS 野生型 (p=0.0004)、変異型 (p<0.0001) ともにTAS-102群で有意に優れていた。
■バイオマーカー解析 (#6099)
本試験の登録症例のうち150例 (TAS-102群: 99例、placebo群: 51例) で、IHCによるTK1およびTPの解析が可能であった。TK1 H-scoreの中央値は両群とも115.0、TP H-scoreの中央値はTAS-102群で12.5、placebo群では15.0であり、両群に有意な差は認められなかった。
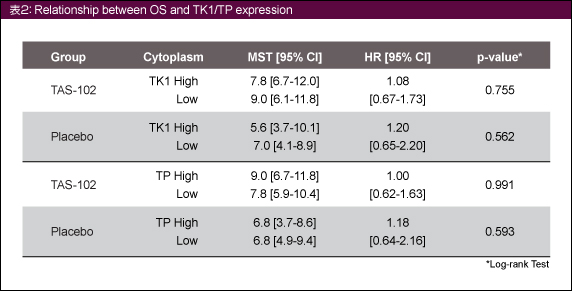
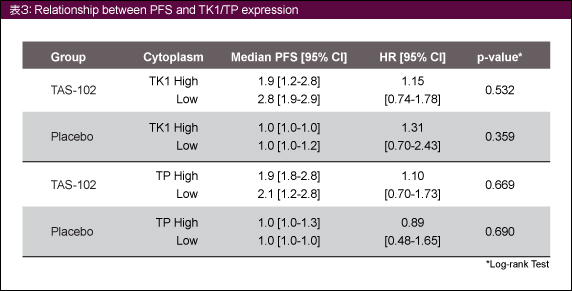
TK1とTPの発現レベルと臨床転帰 (OS、PFS) を表2、3に示す。両群ともに相関は認められなかった。
本試験の登録症例のうち150例 (TAS-102群: 99例、placebo群: 51例) で、IHCによるTK1およびTPの解析が可能であった。TK1 H-scoreの中央値は両群とも115.0、TP H-scoreの中央値はTAS-102群で12.5、placebo群では15.0であり、両群に有意な差は認められなかった。
TK1とTPの発現レベルと臨床転帰 (OS、PFS) を表2、3に示す。両群ともに相関は認められなかった。
TAS-102は従来の標準化学療法に不応な切除不能進行・再発大腸癌患者においてOSを有意に改善し、忍容性も良好であった。現在、KRAS 遺伝子解析を含めた第III相試験が計画されている。
一方、本報告ではTK1およびTP発現とTAS-102治療における臨床転帰との相関は認められなかった。今後のフォローアップデータをもとにさらなる解析を行い、TK1およびTP発現の効果予測因子としての評価を確認すべきであろう。
一方、本報告ではTK1およびTP発現とTAS-102治療における臨床転帰との相関は認められなかった。今後のフォローアップデータをもとにさらなる解析を行い、TK1およびTP発現の効果予測因子としての評価を確認すべきであろう。
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。

